Teste de avaliação – Estrutura atómica (3)
1. Classifica as seguintes afirmações em verdadeiras (V) ou falsas (F).
_____ O modelo atómico de Rutherford é também conhecido como o modelo do “bolo de passas”.
_____ De acordo com o modelo atómico de Bohr, os eletrões movem-se em torno do núcleo em órbitas bem definidas.
_____ Dalton defendia, no seu modelo atómico, que os átomos de um dado elemento químico eram iguais entre si e indivisíveis.
_____ Segundo o modelo da nuvem eletrónica, os eletrões descrevem órbitas em torno do núcleo do átomo.
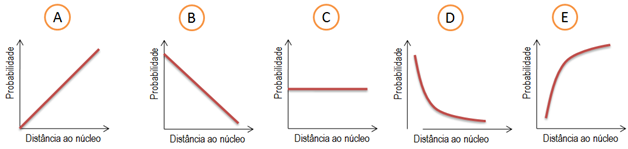
2. Seleciona a opção que indica corretamente qual dos gráficos representa a probabilidade de encontrar o eletrão num determinado ponto do átomo, em função da distância ao núcleo.
3. Considera as representações simbólicas de dois átomos e responde às seguintes questões.
![]()
a. Identifica cada um destes elementos.
b. Qual o número atómico e o número de massa de cada átomo?
c. Qual a carga nuclear e a carga da nuvem eletrónica de cada átomo?
4. Considera o átomo cujo núcleo está representado na imagem e responde às seguintes questões.

Para o referido átomo, indica:
a. o número de protões.
b. o número de eletrões.
c. o número de neutrões.
d. o número de nucleões.
5. Responde à seguinte questão.
Determina a massa atómica relativa do magnésio, tendo em conta os dados contidos na tabela seguinte.
|
Isótopos |
Massa isotópica relativa |
Abundância isotópica |
| Mg-24 | 23,9850 | 78,99 |
| Mg-25 | 24,9858 | 10,00 |
| Mg-26 | 25,9826 | 11,01 |
6. Seleciona a opção correta.
Quando um átomo perde dois eletrões origina um ião com carga…
_____ mononegativa
_____ dipositiva
_____ trinegativa
_____ monopositiva
_____ dnegativa
7. Responde à seguinte questão.
Sabendo que a carga elétrica nuclear de um ião é +5 e que existem 8 eletrões neste ião, calcula a carga elétrica do ião.
8. Seleciona a opção que contém o número máximo de eletrões que o terceiro nível de energia consegue acomodar.
_____ 2
_____ 6
_____ 8
_____ 18
_____ 32
9. Sabe-se que o átomo de um elemento químico X tem 5 eletrões de valência e três níveis de energia preenchidos ou em preenchimento. Escreve a sua distribuição eletrónica.
10. Considera as seguintes representações simbólicas de alguns átomos e responde à seguinte questão.
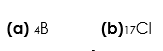
Indica, justificando, que ião cada um dos átomos tende a formar.
Notas:
- Se tiveres alguma dúvida ou algo que aches que devemos melhorar entra em contacto connosco.
- Se detectares algum erro nos apontamentos, podes reportar através do nosso e-mail – [email protected] porque queremos estar constantemente a melhorar para ti.
- Se queres ver os teus testes e/ou trabalhos expostos na nossa página então podes enviá-los para [email protected].
- Os conteúdos da nossa página vão sendo actualizados porque estamos constantemente a melhorá-la.
Aviso:
O Bem Explicado – Centro de Explicações Lda. é um centro de explicações com sede no concelho de Loures. A nossa página surgiu inicialmente para servir como base de dados de todo o material que fomos elaborando ao longo dos anos mas posteriormente reparamos na grande procura por parte de alunos, professores e encarregados de educação. Surgiu assim uma oportunidade de ajudar todos aqueles que não podiam frequentar o nosso espaço físico, ou por dificuldades financeiras ou pela distância.
O nosso principal objectivo é ajudar-te no teu percurso escolar. Sendo assim disponibilizamos os nossos conteúdos de forma gratuita (até ao 9º Ano) e, para que isso continue a acontecer, agradecemos que não haja qualquer cópia ou reprodução dos conteúdos elaborados pelo “Bem Explicado – Centro de Explicações Lda.” porque isso fará com que este projecto termine.
Sendo assim, agradecemos que colabores connosco para que possamos continuar a ajudar-te neste teu grande percurso!
Bem Explicado – Porque o nosso objectivo é o teu Sucesso escolar!

